O efeito dos campos magnéticos na ocorrência e progressão do tumor: avanços recentes
Resumo
As malignidades são a principal ameaça à saúde humana em todo o mundo. Apesar do rápido desenvolvimento dos tratamentos, o prognóstico e o resultado ruins ainda são comuns. Os campos magnéticos têm mostrado bons efeitos antitumorais, tanto em vitro e in vivo , e representam um potencial tratamento não invasivo; no entanto, os mecanismos moleculares subjacentes específicos permanecem obscuros. Aqui, revisamos estudos recentes sobre campos magnéticos e seus efeitos em tumores em três níveis diferentes: organismal, celular e molecular. No nível organismal, os campos magnéticos suprimem a angiogênese tumoral, a microcirculação e aumentam a resposta imune. No nível celular, os campos magnéticos afetam o crescimento das células tumorais e as funções biológicas , afetando a morfologia celular, a estrutura da membrana celular , o ciclo celular e a função mitocondrial . No nível molecular, os campos magnéticos suprimem os tumores interferindo na síntese de DNA , no nível de espécies reativas de oxigênio , na entrega de moléculas de segundo mensageiro e na orientação dos receptores do fator de crescimento epidérmico . Atualmente, ainda faltam evidências experimentais científicas; portanto, estudos sistemáticos sobre os mecanismos biológicos envolvidos são urgentemente necessários para a futura aplicação de campos magnéticos no tratamento de tumores.
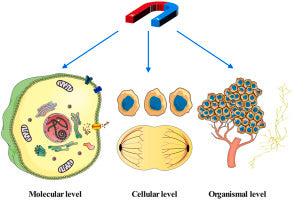
Resumo gráfico
Resumo dos possíveis mecanismos pelos quais os campos magnéticos afetam os tumores.

Introdução
O câncer se tornou uma grande ameaça à saúde humana. A taxa de mortalidade por câncer ainda é muito alta de acordo com as estatísticas globais de câncer de 2021 (Siegel et al., 2021), embora tenha havido um progresso significativo no tratamento do câncer (Bray et al., 2018). A quimioterapia continua sendo a principal escolha para o tratamento do câncer, mas apresenta muitos efeitos colaterais. Por esse motivo, a terapia não invasiva está recebendo mais atenção, incluindo a fisioterapia. Vários tipos de fisioterapia têm sido gradualmente aplicados ao tratamento de tumores, como eletroterapia, terapias fotocinéticas, térmicas, magnéticas, ultrassônicas e de micro-ondas, e radioterapia (Mantso et al., 2016; Schildkopf et al., 2010; Correia et al., 2015; Allison et al., 2011; Qu et al., 2012; Eltejaei et al., 2021; Sachsman et al., 2015; Satkauskas et al., 2005; Chen et al., 2010). Entre estas, a terapia magnética tem recebido atenção considerável (Zhang et al., 2017a).
Os ímãs têm sido usados na cura de doenças há mais de dois mil anos. Recentemente, a terapia magnética tem sido gradualmente aplicada a tratamentos clínicos, como regeneração de nervos periféricos (Suszyński et al., 2014), osteonecrose (Ding et al., 2011), redução da dor (Zhu et al., 2017; Kiss et al., 2013; Eccles, 2005a, 2005b; Schuster e Rapoport, 2016), regulação da função muscular (Bergman et al., 2004; Chaloupka et al., 2002), anti-inflamatório (Juhász et al., 2014) e promoção da cicatrização de feridas (Zhao et al., 2017; Lv et al., 2021; Shang et al., 2019; Strauch et al., 2007; Jing et al., 2010). Comparado com outros tratamentos, os campos magnéticos têm a vantagem de serem não invasivos, seguros, altamente eficientes, baratos e sem risco de infecção ou cicatrizes.
Com base nas características do campo magnético gerado (MF), os MFs podem ser classificados em campo magnético constante (CMF) ou campo magnético dinâmico (DMF). Um CMF também é conhecido como campo magnético estático (SMF) ou campo magnetostático (MSF), que pode ser gerado por ímãs permanentes ou bobinas solenóides com correntes unidirecionais. De acordo com a intensidade do campo magnético, os CMFs podem ser classificados em MFs fracos (<1 mT), médios (1 mT–1 T), fortes (1–5 T) e ultrafortes (>5 T) (Hunt et al., 2009; Van Huizen et al., 2019; Mild et al., 2002). O DMF varia com o tempo e pode ser classificado como campo magnético alternado (AMF), campo magnético pulsado (PMF), campo magnético pulsante (PuMF) e campo geomagnético (GMF) de acordo com o modo de produção do campo magnético. AMFs são gerados por uma bobina eletromagnética com uma corrente de uma certa frequência, ou por um ímã com movimento regular. PMFs, PuMFs e GMFs são produzidos por uma bobina eletromagnética com uma corrente pulsada, fonte de alimentação CA e Terra e ionosfera, respectivamente (Hristov e Perez, 2011; Hildebrandt et al., 2002; Jedrzejczak-Silicka et al., 2002).
Atualmente, a pesquisa está focada principalmente em MFs com parâmetros fixos (Dini e Abbro, 2005; Zhang et al., 2017b), incluindo SMFs, ou MFs oscilantes induzidos por uma bobina eletromagnética com uma única orientação fixa. Estudos preliminares mostraram que MFs podem afetar a morfologia das células tumorais, estrutura da membrana, metabolismo celular, crescimento, adesão, resposta imune e microcirculação. Na maioria dos estudos, esse efeito dominó foi determinado usando um único parâmetro MF ou um tipo limitado de células tumorais. Zablotskii et al. descobriram que a suscetibilidade magnética das células tumorais diferia devido aos seus diferentes conteúdos celulares (Zhu et al., 2017). Portanto, os efeitos biológicos de um MF nas células tumorais dependem de vários parâmetros MF, como intensidade, frequência e duração da exposição. O tipo de célula tumoral também é extremamente importante, mas ainda faltam investigações sistemáticas.
Embora haja evidências crescentes de que os MFs podem inibir a progressão do tumor, o mecanismo subjacente ainda é pouco compreendido. Portanto, revisamos sistematicamente o progresso neste campo, e os possíveis efeitos biológicos dos MFs em tumores foram analisados em três níveis diferentes, a saber, organismal, celular e molecular. Este estudo fornece uma base teórica para a supressão do crescimento do tumor por MF e será útil para a aplicação racional dos MFs no tratamento de tumores no futuro.
Trechos de seção
Sistema imunológico
A ocorrência e progressão de tumores estão intimamente relacionadas ao sistema imunológico. Sob um MF, um grande número de células imunes foi encontrado crescendo perto de sarcomas; portanto, especulou-se que os MFs poderiam elevar a atividade das células imunes e promover a fagocitose de corpos apoptóticos de células imunes, induzindo assim a morte de células tumorais. Gong et al. mostraram que a atividade das células NK esplênicas em camundongos xenograftados SP2/0 aumentou, e a IL-1 dos macrófagos aumentou significativamente após a exposição
Morfologia celular
A morfologia celular é fundamental para todos os movimentos vitais e varia sob MFs. Dini et al. encontraram bolhas na membrana celular U937, uma superfície celular áspera resultante da exposição a um SMF de 6 mT por 12 h (Dini et al., 2009). Após 96 h de exposição a um EMF de 50 Hz de 0,23 mT ou 1,32 mT, tanto o número de células quanto o coeficiente de polarização das células de feocromocitoma PC12 aumentaram significativamente no grupo EMF de 0,23 mT em comparação com o controle, enquanto o oposto ocorreu no EMF de 1,32 mT
Síntese de DNA
Muitos estudos descobriram que os DMFs podem danificar seletivamente o DNA das células tumorais, inibindo assim sua proliferação. Wolf et al. descobriram que os EMFs de frequência extremamente baixa podem quebrar os filamentos de DNA das células tumorais. Alguns estudos mostraram que os EMFs de baixa potência de 0,1–40 MHz também inibiram a proliferação de células tumorais da vesícula biliar ao quebrar os filamentos de DNA, e que o dano ao DNA foi correlacionado de forma não linear com a frequência do MF. A razão nucleocitoplasmática (N/P) é um indicador importante para a
Conclusões e perspectivas
Em resumo, sabe-se que os efeitos biológicos dos MFs sobre tumores ocorrem nos níveis organismal, celular e molecular. No nível organismal, os MFs aumentam a atividade das células imunes, especialmente as células NK, T e B. A angiogênese tumoral também é perturbada sob MFs, com diminuição da densidade e do diâmetro dos vasos, da taxa de fluxo de hemácias e da velocidade do fluxo sanguíneo. Além disso, aumentou significativamente o vazamento de microvasos tumorais, prejudicando ainda mais o endotélio vascular tumoral.
Declaração de conflito de interesses
Todos os autores não declararam relacionamentos relevantes. O autor declarou não haver potenciais conflitos de interesse com relação à pesquisa, autoria e publicação deste artigo.
Agradecimentos
Este trabalho foi apoiado pela Fundação Nacional de Ciências Naturais da China [números de subvenções 52177226 , 82172063 ]; o Programa de P&D da Província de Shaanxi [número da bolsa 2021 KW-62 ]; o Programa de Apoio à Capacidade de Inovação de Shaanxi [número da bolsa 2020TD-042 ]; o Fundação de Ciência Pós-Doutoral da China [número da bolsa 2019T120948 ]; o Fundação de Ciência Pós-Doutoral de Shaanxi [número da bolsa 2018BSHEDZZ02 ]; o Fundação de Inovação para Dissertação de Doutorado da Northwestern Polytechnical University [conceder